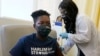
ABD Gıda ve İlaç Dairesi (FDA) Pfizer/BioNTech'in geliştirdiği Corona virüsü aşısının 65 yaş ve üzerindekiler, ağır hastalık riski taşıyan tüm kişiler ve virüse düzenli olarak maruz kalanlar için üçüncü takviye dozunun uygulanmasını onayladı.
FDA'in bu kararı, ikinci doz Pfizer/BioNTech aşılarını en az altı ay önce olan milyonlarca Amerikalı için üçüncü doz aşıların bu haftadan itibaren yapılmaya başlanmasının önünü açacak. FDA Başkan Vekili Janet Woodcock, aşının acil kullanım onayındaki değişikliğin, sağlık çalışanları, öğretmenler, çocuk bakım merkezlerindeki çalışanlar, süpermarket, evsiz barınakları ve hapishane çalışanlarının takviye dozlarla aşılanmasını sağlayacağını söyledi.
Pfizer, FDA'in takviye doz aşıları 16 yaş ve üzerindeki herkes için onaylaması talebinde bulunmuş ve geçen hafta, bağımsız danışmanlardan oluşan kurula, aşının sağladığı bağışıklığın zaman içinde azaldığını gösteren verileri sunmuştu.
Danışma kurulu, takviye aşıların risk grubunda olup olmadıklarını gözetmeksizin herkese yapılması gerektiği iddiasına karşı tavır aldı. Ancak kanıtlar, takviye dozların yaşlılar ve risk altında olanlar için faydalı olduğunu ortaya koyuyor.
Ulusal Bulaşıcı Hastalıklar Vakfı'nın tıp direktörü Dr. William Schaffner, FDA'in açıklamasının, danışma kurulunun tavsiyelerine kıyasla kimlere takviye doz aşı yapılması gerektiği konusunda daha kapsayıcı bir rehber sunduğunu söyledi.
ABD Hastalık Kontrol ve Önleme Merkezleri (CDC) bünyesindeki Aşı Uygulamaları Danışma Komitesi de FDA kararından saatler sonra aşının 65 yaş üstü ile belli hastalık ve kronik rahatsızlıklara bulunanlara, güçlendirici dozu tavsiye etti. Böylelikle gelecek haftadan itibaren üçüncü doz aşılamaları başlayacak.
Başkan Joe Biden ve aralarında FDA Başkan Vekili Dr. Janet Woodcock'un da bulunduğu sekiz sağlık yetkilisi, Ağustos ayında, 16 yaş ve üzerindekiler için takviye aşı kampanyası başlatmayı hedeflediğini açıklamıştı.
Ancak danışma kurulu, herkese takviye aşı gerektiği yönünde yeterli kanıt olmadığını bildirdi ve daha fazla güvenlik verisi talebinde bulundu. FDA, danışma kurulunun tavsiyesine uymak zorunda olmamakla birlikte genellikle kurulun tavsiyeleri çizgisinde karar alıyor.
FDA, ileride takviye aşılara daha kapsamlı onay verilmesi konusunu yeniden ele alabilir.
Pfizer CEO'su Albert Bourla, "FDA'den Covid-19 takviye aşılarının ruhsatlandırılması için gelecek ilk karar, bu hastalıkla mücadelede kritik bir eşik olacak" dedi.
Aralarında İsrail ve İngiltere'nin de olduğu bazı ülkeler, takviye aşı kampanyalarına bir süredir devam ediyor. CDC verilerine göre ABD'de geçen ay bağışıklık sistemi zayıf kişiler için takviye aşı uygulanabileceği yönünde çıkan karardan sonra 2 milyondan fazla Amerikalı, üçüncü doz aşılarını yaptırdı.